缺氧诱导因子Hypoxia induced factor 1 α (HIF-1α)是肿瘤适应缺氧微环境的重要调节因子。2019年美国科学家William G. Kaelin、Gregg. L. Semenza以及英国科学家Sir Peter J. Ratcliffe三位科学家凭借对“氧感知通路”的深入研究,揭露了氧水平对细胞代谢和生理功能的影响,获得诺贝尔生理学与医学奖。HIFs是一种随着细胞内氧浓度变化而调节基因表达的转录激活因子,是一个异二聚体,由氧调节的α亚单位和稳定的β亚单位组成。目前已经超过100个基因受HIFs尤其是HIF1α的转录调控,这些基因编码的蛋白主要对肿瘤细胞血管的生成,葡萄糖转运与糖酵解酶、细胞增殖与存活及侵袭和转移发挥着重要的作用。而HIF1α/p300是调控这些下游基因表达的重要复合物,靶向HIF1α/p300蛋白蛋白相互作用展开抑制剂的开发成为抗肿瘤药物研究的又一热点。
近日,李子刚/尹丰课题组利用本课题组开发的末端天冬氨酸的螺旋诱导的稳定多肽方法,筛选出了具有更高亲和力、良好细胞穿膜性和血清稳定性的多肽抑制剂,其成果发表在药物化学期刊《Journalof Medicinal Chemistry》上,题目为“Potent inhibition of HIF1α and p300 interaction by a constrained peptide derived from CITED2”。与已经报道的HIF1α衍生的多肽抑制剂不同,该工作从HIF1α的竞争蛋白CITED2蛋白出发,截取其与p300结合的最小序列片段进行了详细地研究。经过一系列的截短筛选和突变优化,最后得到一条具有更高亲和力和良好细胞穿膜性的线性多肽,并在此基础上使用末端天冬氨酸的螺旋诱导的稳定多肽方法,对线性多肽进行关环从而稳定其二级构象。实验结果表明,稳定多肽相对于线性肽在血清中更不易被降解,低氧条件下具有更强地抑制下游基因表达的效果。这一发现也为靶向HIF1α/p300PPI提供又一个可行的策略,为抑制相关肿瘤的生长及癌症的治疗提供了新的可能性。
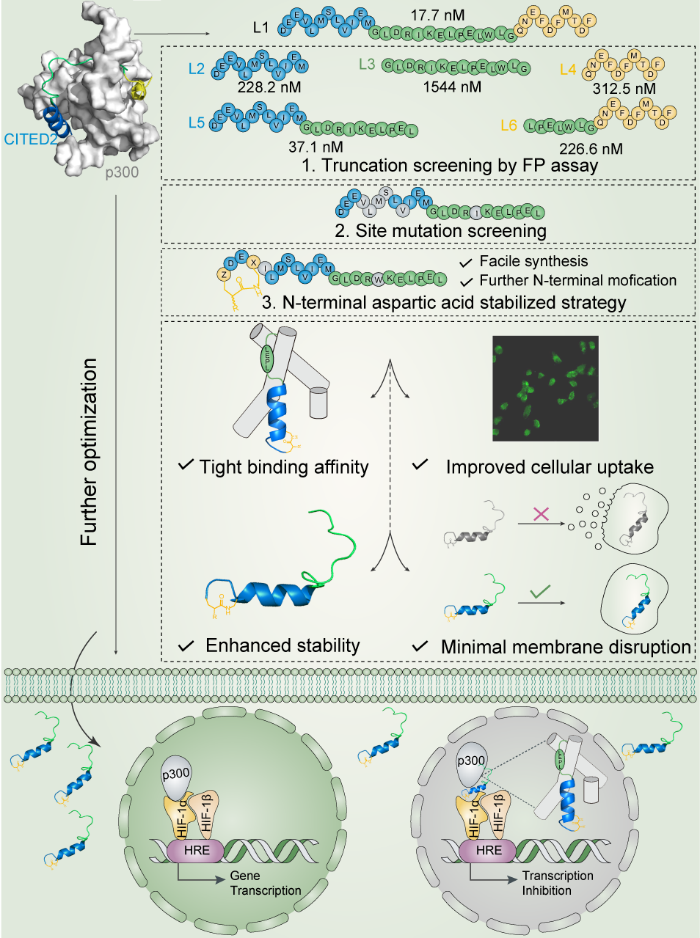
图1:多肽筛选示意图。
北京大学深圳研究生院秦璇博士,博士研究生陈海灵为该论文的并列第一作者,北京大学深圳研究生院李子刚教授、尹丰研究员以及拜耳公司的Donald Bierer为该论文的共同通讯作者。该研究得到了以上工作得到了国家科技部、国家自然科学基金、广东自然科学基金、深圳市科技创新委员会及中国博后科学基金的支持。
论文链接:https://doi.org/10.1021/acs.jmedchem.1c01043